Tìm hiểu về cấu trúc nhựa trao đổi ion
Nhựa trao đổi ion là các polymer mà trên đó các nhóm chức được gắn vào. Trong bài viết này chúng tôi sẽ đi vào chi tiếu cấu trúc hóa học của ma trận nhựa, các nhóm chức và quá trình hóa học tổng thể hoặc sản xuất nhựa trao đổi ion
Nhựa trao đổi ion được sản xuất theo nhiều bước trong đó 2 bước chính là:
- Polyme hóa ma trận nhựa
- Chức năng: các nhóm trao đổi ion được gắn vào ma trận
- Nhựa trao đổi ion là gì – Các loại nhựa trao đổi ion
- Nhựa trao đổi anion là gì
Ma trận nhựa trao đổi ion
Khoảng 90% tất cả các loại nhựa trao đổi ion được dựa trên một ma trận polystyrenic. Khối được sử dụng để tạo ra bộ khung nhựa này là monomer styrene, một hợp chất thơm còn được gọi là vinylbenzene. Dưới đây là các công thức hóa học:
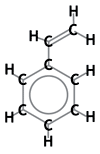
Công thức hóa học của styren
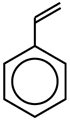
Công thức đơn giản của styrene
Liên kết đôi vinyl của phân tử này cho phép trùng hợp. Hình ảnh tiếp theo cho thấy styrene trùng hợp, mặc dù chỉ có 4 nhóm styrene có thể nhìn thấy. Trong thực tế, hàng triệu nhóm được gắn kết với nhau trong chuỗi rất dài.
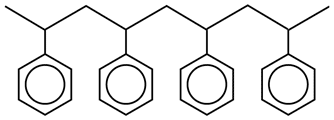
Một phần nhỏ của chuỗi polystyrene
Các chuỗi polymer tuyến tính thu được bị vướng vào nhau nhưng có ít sức mạnh vật lý: chúng tương đối mềm và sau khi kích hoạt có thể chúng sẽ tan trong nước. Để tạo cho polymer một cấu trúc 3 chiều ổn định hơn, các chuỗi polystyrene được liên kết chéo với một phân tử khác tại thời điểm trùng hợp. Phân tử liên kết ngang phải có khả năng trùng hợp ở 2 hoặc 3 đầu. Liên kết chéo phổ biến nhất là divinyl benzene (viết tắt là DVB)
Quá trình trùng hợp thường được thực hiện trong môi trường huyền phù, hoặc trong các lò phản ứng khuấy (trùng hợp mẻ) hoặc trong thiết bị “phun” đặc biệt. Các polyme được hình thành là các hạt hình cầu rất nhỏ (đường kính 200 đến 500). Quá trình phun tạo ra các kích thước hạt rất đồng đều, trong khi trùng hợp hàng loạt dẫn đến các kích thước hạt khác nhau với phân bố kích thước hạt gần Gaussian. Những hạt này sẽ phồng lên với kích thước từ 300 đến 1200 Pha trong các bước chức năng hóa và hydrat hóa tiếp theo
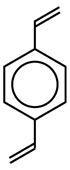
Divynylbenzene(DVB)
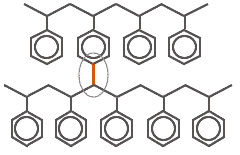
Polystyrene liên kết ngang
Liên kết thứ hai của phân tử DVB được thể hiện bằng màu đỏ và gắn vào chuỗi polystyrene tuyến tính tiếp theo.Càng nhiều DVB được thêm vào hỗn hợp phản ứng ban đầu, polymer càng cứng.
Hầu hết các loại nhựa trao đổi ion được trùng hợp theo cách thu được các hạt hình cầu . Điều này có thể xảy ra hoặc trong một lò phản ứng khuấy hoặc với một quá trình phun. Trong trường hợp sau, kích thước hạt rất đồng đều.
Gel và cấu trúc nhựa macropious
Trong quy trình trùng hợp được mô tả ở trên, liên kết chéo được phân phối đều hoặc ít hơn trong toàn bộ ma trận. Các khoảng trống giữa các chuỗi polystyrene được gọi là lỗ chân lông . Chúng rất nhỏ và kích thước của chúng chỉ vài Å, nhưng kích thước tương đối không đổi: ma trận có cấu trúc tinh thể giả, tương tự như thủy tinh, và kết quả là các hạt resiin trao đổi ion thành phẩm trong suốt . Trong hình dưới đây, các chuỗi polystyrene được hiển thị bằng màu xanh mà không có các chi tiết hóa học thơm và “các đường nối” được hình thành bởi DVB được hiển thị màu đỏ.
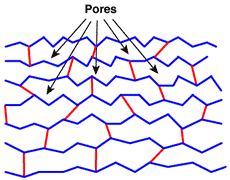
Cấu trúc gel
Có một giới hạn về số lượng DVB có thể được sử dụng trong các loại nhựa gel: quá nhiều DVB tạo ra cấu trúc với các lỗ rất nhỏ, trong sản phẩm cuối cùng có thể là một bất lợi, vì các ion lớn hơn không thể đi vào hạt nhựa. Ngoài ra, các polyme liên kết ngang rất khó kích hoạt.
Để khắc phục vấn đề này, nhựa macropious đã được phát minh vào những năm 1960. Ý tưởng là tạo ra độ xốp nhân tạo trong ma trận ba chiều. Để đạt được hiệu quả này, một thành phần thứ ba – được gọi là porogen hoặc bộ mở rộng pha – được kết hợp trong hỗn hợp phản ứng, không phản ứng với các monome, mà chỉ chiếm chỗ trong hệ thống. Sau khi phản ứng trùng hợp kết thúc, porogen được rửa sạch và để lại các lỗ rỗng trong cấu trúc polymer. Đây là những macropores .
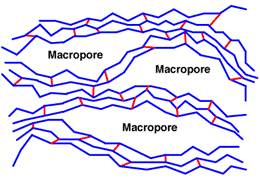
Cấu trúc vĩ mô
Các loại nhựa macropious có độ xốp gấp đôi: các lỗ nhỏ của chính ma trận và các macropores lớn được tạo ra bởi bộ mở rộng pha. Các loại nhựa cuối cùng là mờ đục . Chúng rất ổn định, vì ma trận thường có liên kết chéo cao. Chúng cũng rất xốp, do đó có thể trao đổi các ion lớn.
Kích thước lỗ hạt
Các loại nhựa trao đổi ion được hydrat hóa có chức năng có kích thước lỗ hạt khoảng 1 đến 2nm (10 đến 20), trong khi các loại nhựa macropious, ngoài các lỗ gel nhỏ của chúng, có các macropores với kích thước khoảng 20 đến 100nm (200 đến 1000 Å). Để so sánh, các ion vô cơ ngậm nước có kích thước khoảng 0,2 đến 0,5nm. Các ion hữu cơ có thể lớn hơn thế nhiều.
Chức năng của polymer
Polyme được mô tả ở trên phải được kích hoạt để chuyển các hạt nhựa thành nhựa trao đổi ion.
Nhựa trao đổi cation axit mạnh
Việc kích hoạt rất đơn giản về mặt hóa học: đó là phản ứng sulphonation . các hạt polystyrene được tiếp xúc ở nhiệt độ cao với axit sulfuric đậm đặc. Sản phẩm là một polystyrene sulphonate, là một axit mạnh.
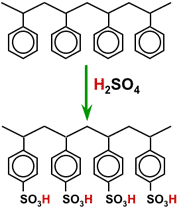
Sulphonation
Sau khi sunfon hóa, nhựa được rửa để loại bỏ axit sulfuric dư thừa. Bước hydrat hóa này là một hoạt động tinh tế, vì nó làm cho các hạt nhựa bị phồng lên (các nhóm chức năng được hydrat hóa và do đó tăng kích thước). Lực thẩm thấu tương ứng là đáng kể và có thể dẫn đến phá vỡ các hạt thành từng mảnh nếu nó không được thực hiện một cách thận trọng.
Phản ứng này tạo ra nhựa ở dạng hydro. Nếu sản phẩm được sử dụng làm nhựa làm mềm, nó phải được chuyển đổi trong một bước bổ sung thành dạng natri. Điều này có thể được thực hiện với natri cacbonat
Nhựa trao đổi anion cơ bazo mạnh và yếu
Việc kích hoạt phức tạp hơn, vì nó đòi hỏi hai bước liên tiếp. Ngoài ra, các hóa chất được sử dụng đắt hơn, điều này giải thích rằng nhựa trao đổi anion đắt hơn đáng kể so với nhựa SAC. Bước đầu tiên được gọi là chloromethylation , và là một phản ứng giữa các hạt polymer và chloromethyl methylether (là một hóa chất rất nguy hiểm)
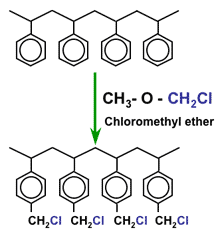
Clorua hóa
Sản phẩm có các nhóm clorua, nhưng đây là các hóa trị, không bị ion hóa. Ở giai đoạn này, chúng ta chưa có nhựa trao đổi anion. Bước thứ hai của quá trình kích hoạt là một quá trình amin hóa , trong đó clorua hóa trị được thay thế bằng một amin.
Amination
Hình ảnh cho thấy hai trường hợp amination. Sản phẩm này là muối amoni clorua bậc bốn. Trong phản ứng đầu tiên, amin được sử dụng là trimethylamine. Theo quy ước, nhựa SBA được sản xuất với trimethylamine được gọi là Loại 1 . Trong phản ứng thứ hai, amin là dimethylethanolamine và sản phẩm được gọi là Loại 2 . Khi được sản xuất, nhựa SBA ở dạng clorua (Cl – ). Chúng thường được lưu trữ và vận chuyển ở dạng này, ổn định hơn dạng OH và phải được tái sinh bằng xút trước khi sử dụng trong hệ thống khử khoáng.
Sự tái sinh
Nhựa loại 1 là loại trao đổi bazo mạnh mẽ phổ biến nhất. Nhựa loại 2 có độ bazo thấp hơn loại 1. Điều này dẫn đến khả năng tái sinh tốt hơn (chuyển đổi thành dạng OH) nhưng nhựa loại 2 nhạy hơn với sự suy giảm nhiệt độ và có độ chọn lọc thấp hơn đối với các ion, do đó độ rò rỉ cao hơn phục vụ.
Nhựa trao đổi anion bazo yếu được sản xuất theo cùng một cách, nhưng sử dụng một thứ cấp thay vì một amin bậc ba. Trong hầu hết các trường hợp, dimethylamine (hiển thị bên trái) được sử dụng. Sản phẩm này là nhựa trao đổi ion ở dạng hydrochloric, được tái sinh thành dạng bazơ miễn phí để cung cấp. Nhựa WBA này được hiển thị bên phải. Ở dạng tái sinh, nhựa WBA không có các ion trao đổi. Đây là lý do tại sao chúng được cho là ở dạng bazo tự do , không phải ở dạng OH, khi được tái sinh. Họ chỉ có thể loại bỏ axit mạnh khỏi dung dịch, có nghĩa là chúng phải được sử dụng sau khi khử. Tuy nhiên, các amin khác có thể được sử dụng để tạo ra các loại nhựa trao đổi anion đặc biệt, chẳng hạn như các chất chọn lọc nitrat (ở đây trên triethylamine bên trái), borat (N-methyl glucamine, xem bên dưới) hoặc perchlorate.
Nhựa trao đổi cation axit yếu
Những loại nhựa này không được sản xuất bằng cách kích hoạt hạt polystyrene. Thay vào đó, chúng được làm từ polyme acrylic, hoặc bắt đầu từ acrylonitril hoặc từ metyl acryat
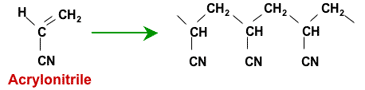
Polyme hóa acrylonitril
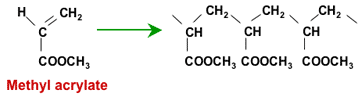
Polyme hóa metyl acryit
Polyme thu được phải được thủy phân để tạo thành các nhóm axit cacboxylic . Polyme polyacrylonitril được thủy phân bằng axit sunfuric, trong khi polyacryit bị thủy phân với xút. Trong cả hai trường hợp, cùng một hợp chất cuối cùng thu được. Ở đây chỉ có thủy phân xút được hiển thị:
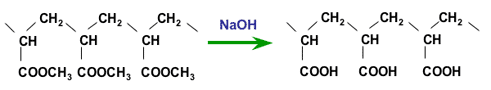
Thủy phân polyacryit bằng xút
Sản phẩm nhựa WAC thu được là một axit yếu, chỉ bị ion hóa một phần trong môi trường trung tính. Độ axit của nó tương tự như axit axetic. Do cấu trúc trọng lượng nhẹ của aliphatic (không thơm) của ma trận, nhựa WAC có mật độ nhóm hoạt động cao hơn so với nhựa dựa trên polystyrene. Điều này dẫn đến khả năng trao đổi ion tổng số cao.
Sau khi phân tách (với một anion kiềm) phản ứng nhựa có thể trao đổi cation. Dưới đây là một ví dụ với natri. Một muối carboxylate được hình thành.
Với các kim loại hóa trị hai, một phức ổn định được hình thành giữa hai nhóm chức, như hình bên trái, điều này giải thích tính chọn lọc cao của nhựa WAC cho các ion này.
Nhựa trao đổi anion acrylic
Nhựa WBA và SBA cũng có thể được tạo ra bắt đầu từ acrylic thay vì copolyme thơm. Bước trùng hợp đầu tiên giống như bước sử dụng nhựa WAC bắt đầu từ metyl acryit, như đã trình bày trong phần trước. Polyacryit sau đó được phản ứng với một di-amin đặc biệt có một amin chính ở một đầu và một amin bậc ba ở đầu kia:
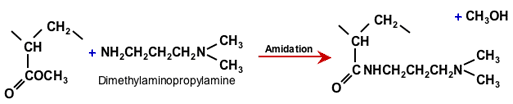
Amid hóa polyacryit với DMAPA
Sản phẩm thu được là nhựa trao đổi anion acrylic cơ bản yếu. Từ đó, một loại nhựa cơ bản mạnh có thể thu được bằng một bước bậc bốn bổ sung bằng cách sử dụng methyl clorua hoặc dimethyl sulphate:
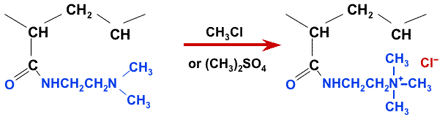
Nhựa acrylic anion ưa nước hơn so với nhựa styrenic, và cho thấy khả năng chống lại sự ô nhiễm hữu cơ vượt trội
Nhựa chelating
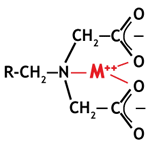 Hầu hết các loại nhựa đặc biệt ở trên thuộc loại chelating. Họ có thể tạo thành phức hợp với kim loại. Tên của chúng có nguồn gốc từ tiếng Hy Lạp có nghĩa là “móng vuốt”, bởi vì các ion kim loại bị bắt giống như trong một móng vuốt. Hình ảnh bên phải cho thấy một kim loại được tạo phức bởi nhóm chức năng imin Zodiacetic của một loại nhựa chelating. Các loại nhựa chelating tạo phức chỉ với các kim loại đa hóa trị. Những phức hợp này rất ổn định. Do đó, các loại nhựa này có tính chọn lọc cao và có khả năng loại bỏ kim loại khỏi dung dịch tốt hơn
Hầu hết các loại nhựa đặc biệt ở trên thuộc loại chelating. Họ có thể tạo thành phức hợp với kim loại. Tên của chúng có nguồn gốc từ tiếng Hy Lạp có nghĩa là “móng vuốt”, bởi vì các ion kim loại bị bắt giống như trong một móng vuốt. Hình ảnh bên phải cho thấy một kim loại được tạo phức bởi nhóm chức năng imin Zodiacetic của một loại nhựa chelating. Các loại nhựa chelating tạo phức chỉ với các kim loại đa hóa trị. Những phức hợp này rất ổn định. Do đó, các loại nhựa này có tính chọn lọc cao và có khả năng loại bỏ kim loại khỏi dung dịch tốt hơn
Các bài viết hay về nhựa trao đổi ion và phương pháp trao đổi ion
- Ứng dụng của trao đổi ion trong các ngành công nghiệp
- Phương pháp xử lý nước cứng làm giảm độ cứng của nước bằng trao đổi ion
- Phương pháp tính toán thiết kế cột trao đổi ion trong xử lý nước
- Các quá trình trao đổi ion cơ bản trong xử lý nước
- Tìm hiểu các thông số hạt nhựa trao đổi ion cho biết điều gì
- Tái sinh nhựa trao đổi ion là gì – Các phương pháp tái sinh nhựa trao đổi ion – Nồng độ hóa chất tái sinh nhựa trao đổi ion

